Кортизол (Гидрокортизон, Cortisol) — узнать цены на анализ и сдать в Симферополе
Синонимы: Анализ крови на кортизол. Hydrocortisone; Compound F.
Краткая характеристика определяемого вещества Кортизол
Кортизол – стероидный гормон, основной представитель глюкокортикоидов, вырабатывается в пучковой зоне коры надпочечников под контролем адренокортикотропного гормона (АКТГ) гипофиза, выработка которого зависит от совокупности поступающих нейрональных и гуморальных стимулов, а также уровня кортизола в крови (по принципу отрицательной обратной связи). В крови большая часть гормона находится в неактивном состоянии: 75% кортизола связано с кортикостероидсвязывающим белком (транскортином), 15% слабо связано с альбумином. Около 10% циркулирует в свободной форме и является биологически активной фракцией гормона. Кортизол подвергается метаболическим превращениям преимущественно в печени, период полураспада составляет 80-110 минут, конъюгаты кортизола выводятся из организма с мочой. Для кортизола характерен суточный ритм секреции с максимумом в утренние часы (6-8 часов) и минимумом в вечернее (22-23 часа) время. Секреция кортизола мало меняется с возрастом. При беременности наблюдается прогрессивный рост концентрации кортизола, связанный с повышением содержания транскортина: в поздние сроки беременности до 2-5-кратного повышения. Суточный ритм выделения этого гормона может нарушаться под воздействием стресса – физического или психологического. В спортивной медицине повышение уровня кортизола в крови расценивается как один из маркеров утомления.
Для кортизола характерен суточный ритм секреции с максимумом в утренние часы (6-8 часов) и минимумом в вечернее (22-23 часа) время. Секреция кортизола мало меняется с возрастом. При беременности наблюдается прогрессивный рост концентрации кортизола, связанный с повышением содержания транскортина: в поздние сроки беременности до 2-5-кратного повышения. Суточный ритм выделения этого гормона может нарушаться под воздействием стресса – физического или психологического. В спортивной медицине повышение уровня кортизола в крови расценивается как один из маркеров утомления.
Глюкокортикоиды прямо или опосредованно регулируют практически все физиологические и биохимические процессы, рецепторы к ним обнаружены во всех тканях организма. Кортизол играет ведущую роль в реакциях организма на стрессовую ситуацию, участвуют в поддержании артериального давления, усиливает катаболизм белков, а также повышает уровень глюкозы в крови. Кортизол обладает мощным противовоспалительным действием. Подавление иммунного ответа связано с ослаблением процессинга антигенов, снижением выработки антител, нарушением различных звеньев лимфопоэза. Гиперчувствительность организма к различным агентам под действием кортизола снижается.
Гиперчувствительность организма к различным агентам под действием кортизола снижается.
Механизмы влияния на жировую ткань разнообразны, и зависят от ее локализации. В конечностях кортизол активирует липолиз, а в верхней половине туловища – к усилению липогенеза. При гиперкортицизме происходит типичное перераспределение подкожно-жировой клетчатки с увеличением объема жировой ткани в области лица, шеи, груди, живота и истончением рук и ног. При избыточной секреции кортизола проявляется его минералокортикоидная активность – наблюдается задержка натрия в организме, отеки и гипокалиемия, а вследствие повышения гломерулярной фильтрации увеличивается диурез. Избыток глюкокортикоидов формирует отрицательный баланс кальция.
С какой целью определяют уровень Кортизола в сыворотке крови
Кортизол является основным глюкокортикоидным гормоном, индикатором функции коры надпочечников. Определение его уровня в крови проводится с целью дифференциальной диагностики синдрома Иценко-Кушинга и болезни Аддисона, скрининга и диагностики первичной и вторичной недостаточности надпочечников, а также для оценки эффективности лечения вышеуказанных патологий.
Синдром Иценко-Кушинга – клинический синдром, который развивается вследствие повышенного содержания глюкокортикоидов в крови. Может развиваться при избыточной эндогенной секреции кортизола при аденоме или карциноме коры надпочечников, АКТГ-секретирующей опухоли локализованной вне гипофиза либо быть следствием длительной терапии глюкокортикоидами, когда их используют как противовоспалительные или иммуносупрессивные средства. Клиническая картина включает характерный тип ожирения (с неравномерным перераспределением подкожно-жировой клетчатки в область верхней части тела и живота), лунообразное лицо, артериальную гипертензию, гирсутизм, нарушение толерантности к углеводам, нарушение репродуктивных функций и нейропсихиатрические симптомы.
Болезнь Иценко-Кушинга представляет собой гипофиз-зависимую форму гиперкортицизма как результат АКТГ-секретирующей аденомы гипофиза.
В дифференциальной диагностике синдрома и болезни Иценко-Кушинга могут быть использованы определение уровня кортизола в сыворотке крови, суточной моче (см. тест № 178) или слюне (см. тест № 1508) АКТГ, а также функциональные пробы и оценку суточных ритмов секреции кортизола (теряется у пациентов с синдромом Иценко-Кушинга). Злоупотребление алкоголем может имитировать по клиническим и биохимическим проявлениям синдром Иценко-Кушинга (изменения обратимы при отказе от алкоголя). Ожирение также может приводить к сходным клиническим проявлениям. В связи с высокой вариабельностью физиологической секреции кортизола и его уровня в сыворотке крови в случайно взятых пробах (в том числе и в утренние часы), в начальном скрининге эндогенного гиперкортицизма предпочтительно использовать оценку суточного выделения кортизола с мочой и/или исследование кортизола в вечерней пробе слюны (собранной в 23 часа вечера). В мочу и слюну попадает преимущественно свободный, не связанный с белками кортизол, и результат таких тестов отражает уровень биологически активного кортизола крови, при использовании суточной мочи – усредненно за сутки, а в пробе слюны – на момент ее сбора вечером.
тест № 178) или слюне (см. тест № 1508) АКТГ, а также функциональные пробы и оценку суточных ритмов секреции кортизола (теряется у пациентов с синдромом Иценко-Кушинга). Злоупотребление алкоголем может имитировать по клиническим и биохимическим проявлениям синдром Иценко-Кушинга (изменения обратимы при отказе от алкоголя). Ожирение также может приводить к сходным клиническим проявлениям. В связи с высокой вариабельностью физиологической секреции кортизола и его уровня в сыворотке крови в случайно взятых пробах (в том числе и в утренние часы), в начальном скрининге эндогенного гиперкортицизма предпочтительно использовать оценку суточного выделения кортизола с мочой и/или исследование кортизола в вечерней пробе слюны (собранной в 23 часа вечера). В мочу и слюну попадает преимущественно свободный, не связанный с белками кортизол, и результат таких тестов отражает уровень биологически активного кортизола крови, при использовании суточной мочи – усредненно за сутки, а в пробе слюны – на момент ее сбора вечером.
Надпочечниковая недостаточность – синдром, обусловленный дефицитом синтеза и секреции кортизола в коре надпочечников.
Болезнь Аддисона (первичная надпочечниковая недостаточность) обусловлена патологией надпочечников в результате воздействия внешних факторов: кровоизлияния, инфекционного, опухолевого, аутоиммунного поражения или после адреналэктомии.
При вторичной и третичной надпочечниковой недостаточности низкий уровень кортизола может быть связан со сниженной секрецией адренокортикотропного гомона (АКТГ) гипофиза или нарушением секреции кортикотропин-рилизинггормона (КРГ) в гипоталамусе. В дифференциальной диагностике надпочечниковой недостаточности применяется определение уровня АКТГ и кортизола базальных и при проведении диагностических проб.
Частой причиной недостаточности надпочечников является состояние, связанное с последствиями фармакологического введения глюкокортикоидов, которые подавляют синтез эндогенных регуляторных гормонов и кортизола.
Врожденная дисфункция коры надпочечников.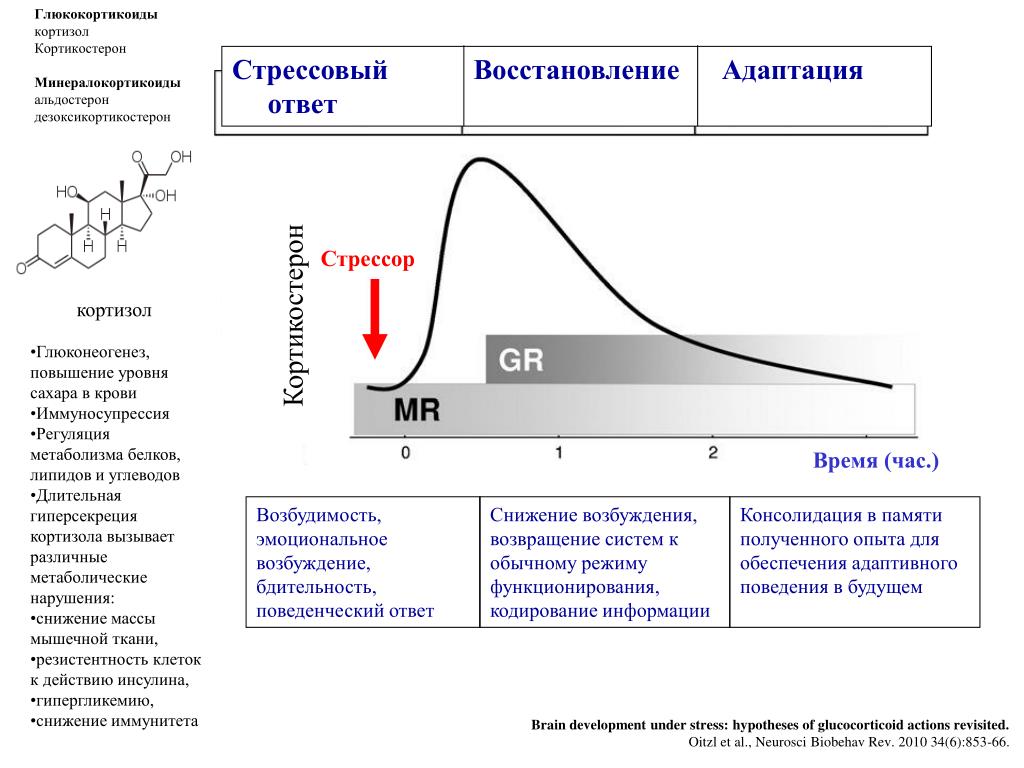 Причиной развития любой формы врожденной дисфункции являются мутации генов, отвечающих за синтез ферментов или транспортных белков, участвующих в биосинтезе кортизола. Наиболее частая форма, встречающаяся более чем в 90% случаев, обусловлена дефицитом фермента 21-гидроксилазы. Нарушение синтеза кортизола вследствие недостаточности фермента 21-гидроксилазы ведет к тому, что по механизму отрицательной обратной связи избыток АКТГ стимулирует корковый слой надпочечников, что вызывает ее гиперплазию. При этом из-за существующего ферментативного блока на пути стероидогенеза накапливаются предшественники кортизола и андрогенов, пути образования которых не заблокированы (17-ОН-прогестерон, ДЭА-SO4, андростендион, тестостерон). У женщин клинические проявления этого синдрома сходны с синдромом поликистозных яичников или идиопатическим гирсутизмом.
Причиной развития любой формы врожденной дисфункции являются мутации генов, отвечающих за синтез ферментов или транспортных белков, участвующих в биосинтезе кортизола. Наиболее частая форма, встречающаяся более чем в 90% случаев, обусловлена дефицитом фермента 21-гидроксилазы. Нарушение синтеза кортизола вследствие недостаточности фермента 21-гидроксилазы ведет к тому, что по механизму отрицательной обратной связи избыток АКТГ стимулирует корковый слой надпочечников, что вызывает ее гиперплазию. При этом из-за существующего ферментативного блока на пути стероидогенеза накапливаются предшественники кортизола и андрогенов, пути образования которых не заблокированы (17-ОН-прогестерон, ДЭА-SO4, андростендион, тестостерон). У женщин клинические проявления этого синдрома сходны с синдромом поликистозных яичников или идиопатическим гирсутизмом.
Пределы определения: 27.6-6599,6 нмоль/л
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Единицы измерения: нмоль/л.
Альтернативные единицы: мкг/100 мл.
Коэффициент пересчета: мкг/100 мл х 27,6 => нмоль/л.
Референсные значения:
утро (до 10 часов): 101,2 — 535,7 нмоль/л;
вечер (после 17 часов): 79,0 — 477,8 нмоль/л.
Трактовка результатов исследования на Кортизол
Повышение значений
- Болезнь Иценко-Кушинга (гипофиз-зависимая).
- Аденома надпочечников.
- Карцинома надпочечников.
- Эктопическая секреция АКТГ.
- Гипогликемия.
- Стресс.
- Беременность.

- Ожирение.
- Депрессия.
- Гипертиреоидизм.
- Прием амфетаминов, кортикотропина, кортизона ацетата, эстрогенов, этанола (внутривенно и перорально), гамма-интерферона, метоксамина, метоклоправида, налоксона, никотина (у курильщиков), пероральных контрацептивов, вазопрессина.
Понижение значений
- Болезнь Аддисона.
- Врожденная недостаточность коры надпочечников (адреногенитальный синдром).
- Гипопитуитаризм (для диагностики необходимы функциональные тесты).
- Гипотиреоз.
- Цирроз печени, гепатиты.
- Лекарственные препараты: аминоглутетимид, беклометазон, бетаметазон, этомидат, кетоконазол, леводопа, карбонат лития, метилпреднизолон, метирапон, морфин, фенитоин, трилостан.
Гормон кортизол — за что отвечает и как быть если он повышен
Кортизол — чем опасно повешенный и пониженный уровень гормона, как делают тест и сколько он стоит
Что такое кортизол
- контроль уровня сахара крови тела
- метаболизм, действуя как противовоспалительное средство
- влияет на память
- контролирует баланс соли и воды в организме
- влияет на кровяное давление
- помогает в развитии плода беременным
- отвечает за запуск процессов, участвующих в родах
Кортизол вырабатывается в коре надпочечников. Уровень кортизола в крови изменяется в течение дня, повышается утром, когда мы просыпаемся и падает в течение дня. Это называется суточным ритмом. У людей, которые работают в ночное время, эта модель полностью изменена, поэтому время высвобождения кортизола четко связано с ежедневными шаблонами активности.
Уровень кортизола в крови изменяется в течение дня, повышается утром, когда мы просыпаемся и падает в течение дня. Это называется суточным ритмом. У людей, которые работают в ночное время, эта модель полностью изменена, поэтому время высвобождения кортизола четко связано с ежедневными шаблонами активности.
Если повышен уровень гормона кортизола
Симптомы повышенного гормона кортизола:
быстрое увеличение веса на лице, груди и животе, что на контрасте со стройными руками и ногами
раскрасневшееся и круглое лицо
высокое кровяное давление
остеопороз
изменения кожи (синяки и фиолетовые растяжки)
мышечная слабость
перепады настроения, которые проявляются в виде тревоги, депрессии или раздражительности
повышенная жажда и частое мочеиспускание
Высокий уровень кортизола в течение длительного времени также может привести к отсутствию полового влечения, а у женщин менструации могут стать нерегулярными, менее частыми или вообще прекратиться.
Кроме того, существует связь между повышением или нарушением уровня кортизола и рядом психических заболеваний, таких как тревога и депрессия.
Если понижен уровень гормона кортизола
Слишком мало кортизола может быть связано с проблемой в гипофизе или надпочечниках (болезнь Аддисона). Симптомы могут включать усталость, головокружение, потерю веса, мышечную слабость, изменения настроения и потемнение участков кожи. Без лечения это потенциально опасное для жизни состояние.
При подозрении на синдром Кушинга или болезнь Аддисона необходимо срочно обратиться к врачу эндокринологу.
Как делают анализ на гормон кортизол
Для проведения анализа отбираются пробы слюны. Четыре раза в день пациент собирает слюну в специальную пробирку и указывает точное время забора пробы. Врач дает пояснения, относительно изменений уровня содержания кортизолa в организме, а также рекомендует лечебные процедуры или занятия, которые помогут ему улучшить состояние.
Когда нужно пройти тест на уровень кортизола
При повышенном или пониженном артериальном давлении, при повышенном содержании сахара в крови, при наличии жировых отложений в области талии, снижении мышечной массы, утомляемости, болезненных ощущениях в брюшной полости, появлении пигментных пятен на коже и т. д.
д.
Наряду с содержанием кортизола рекомендовано тестирование на содержание в организме гормона сна мелатонинa — принцип обследования тот же.
Источники и литература:
Барановский, Андрей Юрьевич Болезни нарушенного питания. Лечение и профилактика. Рекомендации профессора-гастроэнтеролога / Барановский Андрей Юрьевич. — М.: Наука и техника, 2020. — 853 c.
Егоров, М. Н. Ожирение / М.Н. Егоров, Л.М. Левитский. — Москва: Огни, 2016. — 306 c
Болезни обмена веществ: моногр. . — М.: Вече, 2016. — 320 c.
Эндокринная система, спорт и двигательная активность. – Киев: Олимпийская литература, 2008. – 600 с.
Самсонова А.В. Гормоны и гипертрофия скелетных мышц человека: учеб. пособие. – СПб: Кинетика, 2019.– 204 с.
Статья проверена экспертом: врач-терапевт Оксана Николаевна Бочаровская подробнее
Физиология, кортизол — StatPearls — Книжная полка NCBI
Лорен Тау; Джаяшри Ганди; Сандип Шарма.
Информация об авторе и организациях
Последнее обновление: 29 августа 2022 г.
Введение
Хотя кортизол широко известен как гормон стресса, он по-разному влияет на различные функции организма. Это основной глюкокортикоид, высвобождаемый из пучковой зоны коры надпочечников. Ось гипоталамус-гипофиз-надпочечники регулирует как выработку, так и секрецию кортизола. Потеря регуляции может привести к нарушениям избытка кортизола, таким как синдром Кушинга, или корковой недостаточности, такой как болезнь Аддисона.
Сотовый уровень
Кортизол, стероидный гормон, синтезируется из холестерина. Синтезируется в пучковой зоне коры надпочечников. Адренокортикотропный гормон (АКТГ), высвобождаемый передней долей гипофиза, увеличивает количество рецепторов ЛПНП и повышает активность холестеролдесмолазы, которая превращает холестерол в прегненолон и является лимитирующей стадией синтеза кортизола.[1] Большинство глюкокортикоидов циркулируют в неактивной форме, связанной либо с кортикостероид-связывающим глобулином (КСГ), либо с альбумином.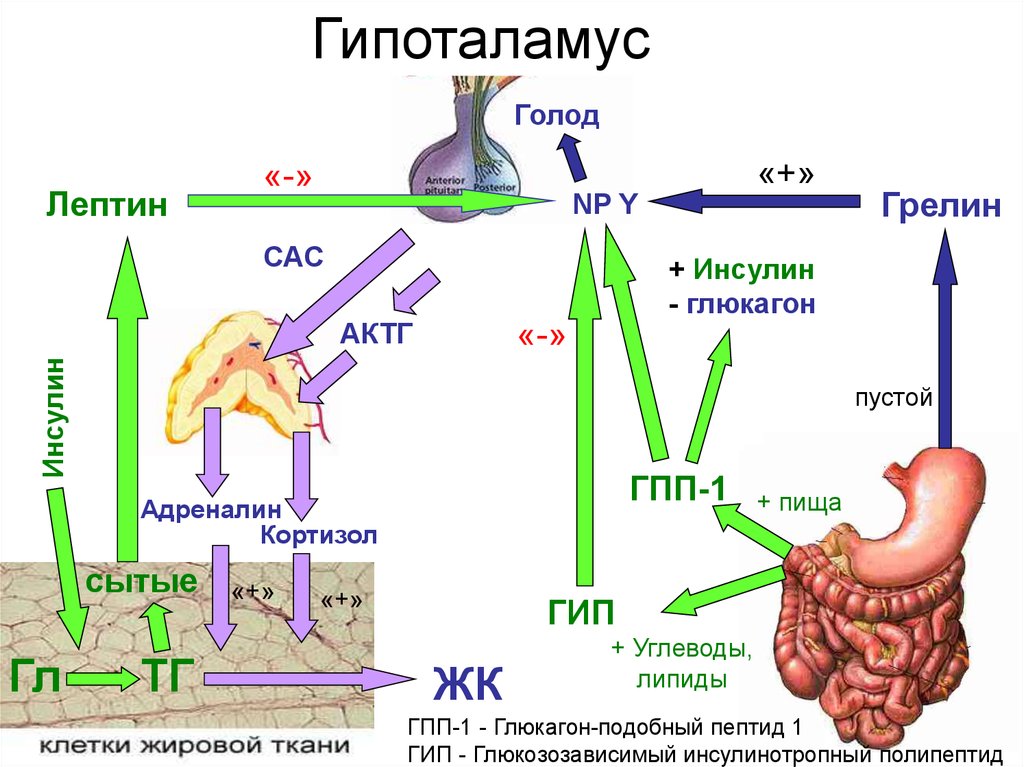 [2] Неактивная форма превращается в активную под действием 11-бета-гидроксистероиддегидрогеназы 1 (11-бета-HSD1) в большинстве тканей, в то время как 11-бета-HSD2 инактивирует кортизол обратно в кортизон в почках и поджелудочной железе.[2]
[2] Неактивная форма превращается в активную под действием 11-бета-гидроксистероиддегидрогеназы 1 (11-бета-HSD1) в большинстве тканей, в то время как 11-бета-HSD2 инактивирует кортизол обратно в кортизон в почках и поджелудочной железе.[2]
Вовлеченные системы органов
Глюкокортикоидные рецепторы присутствуют почти во всех тканях организма. Таким образом, кортизол способен воздействовать почти на все системы органов: 0002 Респираторная
Репродуктивная
Скелетно-мышечная
Покровная
Функция
Кортизол выполняет множество функций в организме человека, например, опосредует реакцию на стресс, регулирует обмен веществ, воспалительную реакцию и иммунную функцию.[4]
Иммунный ответ
Глюкокортикоиды оказывают ряд действий на иммунную систему. Например, они индуцируют апоптоз провоспалительных Т-клеток, подавляют выработку антител В-клетками и уменьшают миграцию нейтрофилов во время воспаления. [3]
[3]
Реакция на стресс
Организм человека постоянно реагирует на внутренние и внешние факторы стресса. Организм обрабатывает стрессовую информацию и вызывает реакцию в зависимости от степени угрозы. Вегетативная нервная система организма делится на симпатическую нервную систему (СНС) и парасимпатическую нервную систему (ПНС). Во время стресса активизируется СНС. СНС отвечает за реакцию «бей или беги», которая вызывает каскад гормональных и физиологических реакций. Миндалевидное тело отвечает за обработку страха, возбуждения и эмоциональных стимулов, чтобы определить соответствующую реакцию. При необходимости миндалевидное тело посылает сигнал стресса в гипоталамус.[5] Затем гипоталамус активирует СНС, а надпочечники выделяют большое количество катехоламинов, таких как адреналин. Это приводит к таким эффектам, как увеличение частоты сердечных сокращений и частоты дыхания. Поскольку тело продолжает воспринимать раздражители как угрозу, гипоталамус активирует ось HPA. Кортизол высвобождается из коры надпочечников и позволяет организму оставаться в состоянии повышенной готовности. В частности, катаболические механизмы кортизола обеспечивают организм энергией.[6]
Кортизол высвобождается из коры надпочечников и позволяет организму оставаться в состоянии повышенной готовности. В частности, катаболические механизмы кортизола обеспечивают организм энергией.[6]
Глюкозный и белковый гомеостаз
Уровень глюкозы в крови управляет ключевыми системными и внутриклеточными путями. Присутствие глюкокортикоидов, таких как кортизол, увеличивает доступ глюкозы крови к мозгу. Кортизол действует на печень, мышцы, жировую ткань и поджелудочную железу. В печени высокие уровни кортизола увеличивают глюконеогенез и снижают синтез гликогена.[7] Глюконеогенез представляет собой метаболический путь, который приводит к образованию глюкозы из глюкогенных аминокислот, лактата или глицерол-3-фосфата, содержащихся в триглицеридах. Глюконеогенез реверсирует гликолиз, цитоплазматический путь, используемый для превращения глюкозы в молекулы пирувата. Этот путь используется для высвобождения энергии посредством реакций фосфорилирования и окисления на уровне субстрата. В отличие от гликолиза, глюконеогенез становится активным, когда организм нуждается в энергии. Мышцы имеют собственный внутренний запас гликогена, что позволяет им быстро реагировать на изменения потребности в АТФ. В присутствии кортизола мышечные клетки снижают поглощение и потребление глюкозы и увеличивают расщепление белка; это обеспечивает глюконеогенез глюкогенными аминокислотами. В жировых тканях кортизол усиливает липолиз. Липолиз — это катаболический процесс, в результате которого высвобождается глицерин и свободные жирные кислоты. Эти свободные жирные кислоты могут использоваться для окисления B и в качестве источника энергии для других клеток, поскольку они продолжают производить глюкозу. Наконец, кортизол действует на поджелудочную железу, снижая уровень инсулина и увеличивая уровень глюкагона. Глюкагон представляет собой пептидный гормон, секретируемый альфа-клетками поджелудочной железы для усиления гликогенолиза в печени, глюконеогенеза в печени, кетогенеза в печени, липолиза, а также для снижения липогенеза.
В отличие от гликолиза, глюконеогенез становится активным, когда организм нуждается в энергии. Мышцы имеют собственный внутренний запас гликогена, что позволяет им быстро реагировать на изменения потребности в АТФ. В присутствии кортизола мышечные клетки снижают поглощение и потребление глюкозы и увеличивают расщепление белка; это обеспечивает глюконеогенез глюкогенными аминокислотами. В жировых тканях кортизол усиливает липолиз. Липолиз — это катаболический процесс, в результате которого высвобождается глицерин и свободные жирные кислоты. Эти свободные жирные кислоты могут использоваться для окисления B и в качестве источника энергии для других клеток, поскольку они продолжают производить глюкозу. Наконец, кортизол действует на поджелудочную железу, снижая уровень инсулина и увеличивая уровень глюкагона. Глюкагон представляет собой пептидный гормон, секретируемый альфа-клетками поджелудочной железы для усиления гликогенолиза в печени, глюконеогенеза в печени, кетогенеза в печени, липолиза, а также для снижения липогенеза. Кортизол усиливает активность глюкагона, адреналина и других катехоламинов.
Кортизол усиливает активность глюкагона, адреналина и других катехоламинов.
Механизм
Высвобождение кортизола находится под контролем оси гипоталамус-гипофиз-надпочечники (ГГН). Кортикотропин-рилизинг-гормон (CRH) высвобождается паравентрикулярным ядром (PVN) гипоталамуса.[2] Затем он действует на переднюю долю гипофиза, высвобождая адренокортикотропный гормон (АКТГ), который впоследствии действует на кору надпочечников. В петле отрицательной обратной связи достаточное количество кортизола ингибирует высвобождение как АКТГ, так и КРГ. Ось HPA следует циркадному ритму. Таким образом, уровень кортизола будет высоким утром и низким ночью [2].
Стероидные гормоны, такие как кортизол, являются первичными мессенджерами. Они могут проникать через цитоплазматическую мембрану благодаря своим жирорастворимым свойствам. Клеточные мембраны состоят из двойных слоев фосфолипидов; они предотвращают прохождение жиронерастворимых молекул. Как только кортизол проходит через клеточную мембрану и проникает в клетку, он связывается со специфическими рецепторами в цитоплазме. В отсутствие кортизола глюкокортикоидный рецептор связывается с белком-шапероном Hsp90 в цитозоле. Связывание кортизола с глюкокортикоидным рецептором диссоциирует Hsp9.0. Затем комплекс кортизол-рецептор проникает в ядро клетки и влияет на транскрипцию генов.
В отсутствие кортизола глюкокортикоидный рецептор связывается с белком-шапероном Hsp90 в цитозоле. Связывание кортизола с глюкокортикоидным рецептором диссоциирует Hsp9.0. Затем комплекс кортизол-рецептор проникает в ядро клетки и влияет на транскрипцию генов.
Связанные тесты
Считается, что уровни кортизола в слюне коррелируют с уровнями свободного кортизола в плазме и сыворотке.[6] Ночное измерение кортизола в слюне используется в качестве начального диагностического теста на синдром Кушинга, синдром избытка глюкокортикоидов.[6] Поскольку уровни кортизола должны быть высокими по утрам, одним из первоначальных диагностических тестов на болезнь Аддисона является проверка уровня кортизола в сыворотке рано утром.[9]]
Клиническое значение
Уровень кортизола в организме постоянно контролируется для поддержания гомеостаза. Нерегулируемые уровни могут быть вредными.
Гиперкортицизм
Синдром Кушинга возникает, когда организм человека подвергается воздействию высоких уровней кортизола в течение длительного периода времени. Различные этиологии синдрома Кушинга можно разделить на АКТГ-зависимые и АКТГ-независимые. При АКТГ-зависимых подтипах наблюдается избыток АКТГ либо из-за опухоли гипофиза, либо из-за эктопического источника, такого как нейроэндокринная опухоль.[10] В обоих случаях перепроизводство АКТГ стимулирует надпочечники к выработке избыточного кортизола. В АКТГ-независимых подтипах есть эндогенная этиология и экзогенная этиология. Эндогенная причина обычно связана с опухолью надпочечников, что приводит к избыточной выработке кортизола. Экзогенная причина связана с чрезмерным использованием пероральных или инъекционных кортикостероидов. Пероральные кортикостероиды, такие как преднизолон, увеличивают количество кортизола в организме. Их назначают для облегчения симптомов, связанных с хроническими воспалительными заболеваниями, такими как системная эритематозная волчанка (СКВ) и ревматоидный артрит. Симптомы синдрома Кушинга зависят от того, насколько повышен уровень кортизола. Общие признаки и симптомы избытка кортизола включают увеличение веса (особенно на лице и животе), жировые отложения между лопатками, диабет, гипертонию, гирсутизм у женщин, слабость проксимальных мышц и остеопороз.
Различные этиологии синдрома Кушинга можно разделить на АКТГ-зависимые и АКТГ-независимые. При АКТГ-зависимых подтипах наблюдается избыток АКТГ либо из-за опухоли гипофиза, либо из-за эктопического источника, такого как нейроэндокринная опухоль.[10] В обоих случаях перепроизводство АКТГ стимулирует надпочечники к выработке избыточного кортизола. В АКТГ-независимых подтипах есть эндогенная этиология и экзогенная этиология. Эндогенная причина обычно связана с опухолью надпочечников, что приводит к избыточной выработке кортизола. Экзогенная причина связана с чрезмерным использованием пероральных или инъекционных кортикостероидов. Пероральные кортикостероиды, такие как преднизолон, увеличивают количество кортизола в организме. Их назначают для облегчения симптомов, связанных с хроническими воспалительными заболеваниями, такими как системная эритематозная волчанка (СКВ) и ревматоидный артрит. Симптомы синдрома Кушинга зависят от того, насколько повышен уровень кортизола. Общие признаки и симптомы избытка кортизола включают увеличение веса (особенно на лице и животе), жировые отложения между лопатками, диабет, гипертонию, гирсутизм у женщин, слабость проксимальных мышц и остеопороз. [11] Лечение синдрома Кушинга зависит от причины. Чаще всего лечение проводится с помощью хирургического вмешательства. Однако антагонисты глюкокортикоидных рецепторов также могут применяться при наличии противопоказаний к хирургическому вмешательству.
[11] Лечение синдрома Кушинга зависит от причины. Чаще всего лечение проводится с помощью хирургического вмешательства. Однако антагонисты глюкокортикоидных рецепторов также могут применяться при наличии противопоказаний к хирургическому вмешательству.
Гипокортицизм
Первичная надпочечниковая недостаточность, также известная как болезнь Аддисона, чаще всего вызывается аутоиммунным адреналитом.[9] Другие причины включают злокачественное новообразование, инфекцию или кровоизлияние в надпочечники. Аутоиммунный адреналит возникает в результате того, что организм атакует кору надпочечников.[12] Вторичная недостаточность надпочечников связана с недостаточной продукцией АКТГ передней долей гипофиза. Это может быть вызвано заболеванием гипофиза, но наиболее частая причина связана с подавлением оси HPA из-за хронического приема экзогенных глюкокортикоидов. Третичная надпочечниковая недостаточность возникает из-за отсутствия высвобождения КРГ из гипоталамуса. Симптомы надпочечниковой недостаточности включают утомляемость, потерю веса, гипотонию и гиперпигментацию кожи. [14] Поскольку альдостерона также будет недостаточно, лабораторные результаты покажут гиперкалиемию. Заместительная терапия глюкокортикоидами, например гидрокортизоном, необходима для лечения симптомов гипокортицизма. Важно помнить об увеличении дозировки при острых стрессовых факторах, таких как болезнь или хирургическое вмешательство, чтобы избежать надпочечникового кризиса.[14]
[14] Поскольку альдостерона также будет недостаточно, лабораторные результаты покажут гиперкалиемию. Заместительная терапия глюкокортикоидами, например гидрокортизоном, необходима для лечения симптомов гипокортицизма. Важно помнить об увеличении дозировки при острых стрессовых факторах, таких как болезнь или хирургическое вмешательство, чтобы избежать надпочечникового кризиса.[14]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Ангелуси А., Маргиорис А.Н., Цацанис С. Действие АКТГ на надпочечники. Пришли: Фейнгольд К.Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж., Калра С., Калтсас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы.
 Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342]
Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342]- 2.
Рамамурти С., Сидловски Дж.А. Кортикостероиды: механизмы действия в норме и при заболевании. Реум Дис Клин Норт Ам. 2016 Feb;42(1):15-31, vii. [Бесплатная статья PMC: PMC4662771] [PubMed: 26611548]
- 3.
Kadmiel M, Cidlowski JA. Сигнализация глюкокортикоидных рецепторов в норме и при патологии. Trends Pharmacol Sci. 2013 сен; 34 (9): 518-30. [Бесплатная статья PMC: PMC3951203] [PubMed: 23953592]
- 4.
Oakley RH, Cidlowski JA. Биология глюкокортикоидного рецептора: новые сигнальные механизмы в норме и при патологии. J Аллергия Клин Иммунол. 2013 ноябрь; 132(5):1033-44. [Бесплатная статья PMC: PMC4084612] [PubMed: 24084075]
- 5.
Хакамата Ю., Коми С., Моригути Ю., Изава С., Мотомура Ю., Сато Э., Мизуками С., Ким Ю., Ханакава Т., Иноуэ Ю., Тагая Х. Функциональная связность миндалевидного тела влияет на суточную концентрацию кортизола : предполагаемая связь с тревогой.
 Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810]
Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810]- 6.
Lee DY, Kim E, Choi MH. Технические и клинические аспекты кортизола как биохимического маркера хронического стресса. Отчет BMB, апрель 2015 г.; 48 (4): 209-16. [Бесплатная статья PMC: PMC4436856] [PubMed: 25560699]
- 7.
Kuo T, McQueen A, Chen TC, Wang JC. Регуляция гомеостаза глюкозы глюкокортикоидами. Adv Exp Med Biol. 2015;872:99-126. [Бесплатная статья PMC: PMC6185996] [PubMed: 26215992]
- 8.
Exton JH. Регуляция глюконеогенеза глюкокортикоидами. Моногр Эндокринол. 1979; 12:535-46. [PubMed: 386091]
- 9.
Michels A, Michels N. Болезнь Аддисона: раннее выявление и принципы лечения. Ам семейный врач. 2014 01 апреля; 89(7): 563-8. [PubMed: 24695602]
- 10.
Рафф Х., Кэрролл Т. Синдром Кушинга: от физиологических принципов к диагностике и клиническому лечению.
 Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800]
Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800]- 11.
Лила А.Р., Саратхи В., Джагтап В.С., Бандгар Т., Менон П., Шах Н.С. Синдром Кушинга: поэтапный подход к диагностике. Индийский J Endocrinol Metab. 2011 Октябрь; 15 Дополнение 4 (Приложение 4): S317-21. [Бесплатная статья PMC: PMC3230095] [PubMed: 22145134]
- 12.
Ниари Н., Ниман Л. Надпочечниковая недостаточность: этиология, диагностика и лечение. Curr Opin Endocrinol Diabetes Obes. 2010 июнь;17(3):217-23. [Бесплатная статья PMC: PMC2928659] [PubMed: 20375886]
- 13.
Войцик М., Русала А., Янус Д., Старжик Дж. Б. Вторичная надпочечниковая недостаточность вследствие внутрисуставных инъекций глюкокортикоидов. Индийский педиатр. 2019 15 марта; 56 (3): 242-243. [PubMed: 30954999]
- 14.
Александраки К.И., Санпавитаякул К., Гроссман А. Надпочечниковая недостаточность. Пришли: Фейнгольд К.
 Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж., Калра С., Калтсас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы. Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 7 ноября 2022 г. [PubMed: 25905309]
Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж., Калра С., Калтсас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы. Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 7 ноября 2022 г. [PubMed: 25905309]
Раскрытие информации: Лорен Тау заявляет об отсутствии соответствующих финансовых отношений с неправомочными компаниями.
Раскрытие информации: Джаяшри Ганди заявляет об отсутствии соответствующих финансовых отношений с неправомочными компаниями.
Раскрытие информации: Сандип Шарма заявляет об отсутствии соответствующих финансовых отношений с неправомочными компаниями.
Физиология, кортизол — StatPearls — Книжная полка NCBI
Лорен Тау; Джаяшри Ганди; Сандип Шарма.
Информация об авторе и организациях
Последнее обновление: 29 августа 2022 г.
Введение
Хотя кортизол широко известен как гормон стресса, он по-разному влияет на различные функции организма. Это основной глюкокортикоид, высвобождаемый из пучковой зоны коры надпочечников. Ось гипоталамус-гипофиз-надпочечники регулирует как выработку, так и секрецию кортизола. Потеря регуляции может привести к нарушениям избытка кортизола, таким как синдром Кушинга, или корковой недостаточности, такой как болезнь Аддисона.
Сотовый уровень
Кортизол, стероидный гормон, синтезируется из холестерина. Синтезируется в пучковой зоне коры надпочечников. Адренокортикотропный гормон (АКТГ), высвобождаемый передней долей гипофиза, увеличивает количество рецепторов ЛПНП и повышает активность холестеролдесмолазы, которая превращает холестерол в прегненолон и является лимитирующей стадией синтеза кортизола.[1] Большинство глюкокортикоидов циркулируют в неактивной форме, связанной либо с кортикостероид-связывающим глобулином (КСГ), либо с альбумином. [2] Неактивная форма превращается в активную под действием 11-бета-гидроксистероиддегидрогеназы 1 (11-бета-HSD1) в большинстве тканей, в то время как 11-бета-HSD2 инактивирует кортизол обратно в кортизон в почках и поджелудочной железе.[2]
[2] Неактивная форма превращается в активную под действием 11-бета-гидроксистероиддегидрогеназы 1 (11-бета-HSD1) в большинстве тканей, в то время как 11-бета-HSD2 инактивирует кортизол обратно в кортизон в почках и поджелудочной железе.[2]
Вовлеченные системы органов
Глюкокортикоидные рецепторы присутствуют почти во всех тканях организма. Таким образом, кортизол способен воздействовать почти на все системы органов: 0002 Респираторная
Репродуктивная
Скелетно-мышечная
Покровная
Функция
Кортизол выполняет множество функций в организме человека, например, опосредует реакцию на стресс, регулирует обмен веществ, воспалительную реакцию и иммунную функцию.[4]
Иммунный ответ
Глюкокортикоиды оказывают ряд действий на иммунную систему. Например, они индуцируют апоптоз провоспалительных Т-клеток, подавляют выработку антител В-клетками и уменьшают миграцию нейтрофилов во время воспаления. [3]
[3]
Реакция на стресс
Организм человека постоянно реагирует на внутренние и внешние факторы стресса. Организм обрабатывает стрессовую информацию и вызывает реакцию в зависимости от степени угрозы. Вегетативная нервная система организма делится на симпатическую нервную систему (СНС) и парасимпатическую нервную систему (ПНС). Во время стресса активизируется СНС. СНС отвечает за реакцию «бей или беги», которая вызывает каскад гормональных и физиологических реакций. Миндалевидное тело отвечает за обработку страха, возбуждения и эмоциональных стимулов, чтобы определить соответствующую реакцию. При необходимости миндалевидное тело посылает сигнал стресса в гипоталамус.[5] Затем гипоталамус активирует СНС, а надпочечники выделяют большое количество катехоламинов, таких как адреналин. Это приводит к таким эффектам, как увеличение частоты сердечных сокращений и частоты дыхания. Поскольку тело продолжает воспринимать раздражители как угрозу, гипоталамус активирует ось HPA. Кортизол высвобождается из коры надпочечников и позволяет организму оставаться в состоянии повышенной готовности. В частности, катаболические механизмы кортизола обеспечивают организм энергией.[6]
Кортизол высвобождается из коры надпочечников и позволяет организму оставаться в состоянии повышенной готовности. В частности, катаболические механизмы кортизола обеспечивают организм энергией.[6]
Глюкозный и белковый гомеостаз
Уровень глюкозы в крови управляет ключевыми системными и внутриклеточными путями. Присутствие глюкокортикоидов, таких как кортизол, увеличивает доступ глюкозы крови к мозгу. Кортизол действует на печень, мышцы, жировую ткань и поджелудочную железу. В печени высокие уровни кортизола увеличивают глюконеогенез и снижают синтез гликогена.[7] Глюконеогенез представляет собой метаболический путь, который приводит к образованию глюкозы из глюкогенных аминокислот, лактата или глицерол-3-фосфата, содержащихся в триглицеридах. Глюконеогенез реверсирует гликолиз, цитоплазматический путь, используемый для превращения глюкозы в молекулы пирувата. Этот путь используется для высвобождения энергии посредством реакций фосфорилирования и окисления на уровне субстрата.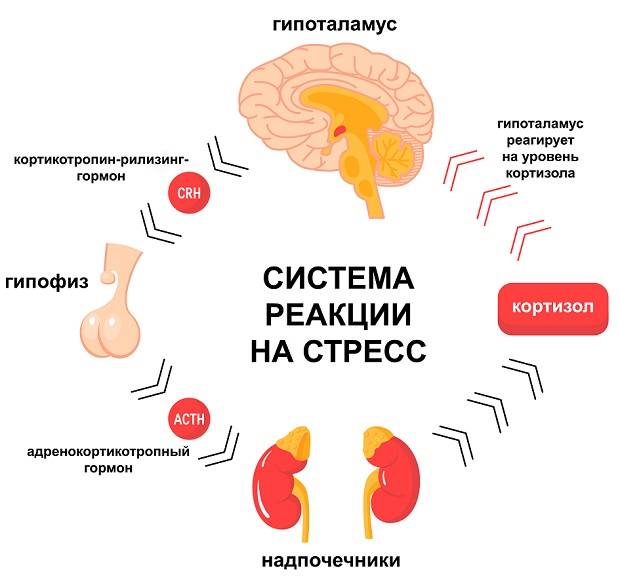 В отличие от гликолиза, глюконеогенез становится активным, когда организм нуждается в энергии. Мышцы имеют собственный внутренний запас гликогена, что позволяет им быстро реагировать на изменения потребности в АТФ. В присутствии кортизола мышечные клетки снижают поглощение и потребление глюкозы и увеличивают расщепление белка; это обеспечивает глюконеогенез глюкогенными аминокислотами. В жировых тканях кортизол усиливает липолиз. Липолиз — это катаболический процесс, в результате которого высвобождается глицерин и свободные жирные кислоты. Эти свободные жирные кислоты могут использоваться для окисления B и в качестве источника энергии для других клеток, поскольку они продолжают производить глюкозу. Наконец, кортизол действует на поджелудочную железу, снижая уровень инсулина и увеличивая уровень глюкагона. Глюкагон представляет собой пептидный гормон, секретируемый альфа-клетками поджелудочной железы для усиления гликогенолиза в печени, глюконеогенеза в печени, кетогенеза в печени, липолиза, а также для снижения липогенеза.
В отличие от гликолиза, глюконеогенез становится активным, когда организм нуждается в энергии. Мышцы имеют собственный внутренний запас гликогена, что позволяет им быстро реагировать на изменения потребности в АТФ. В присутствии кортизола мышечные клетки снижают поглощение и потребление глюкозы и увеличивают расщепление белка; это обеспечивает глюконеогенез глюкогенными аминокислотами. В жировых тканях кортизол усиливает липолиз. Липолиз — это катаболический процесс, в результате которого высвобождается глицерин и свободные жирные кислоты. Эти свободные жирные кислоты могут использоваться для окисления B и в качестве источника энергии для других клеток, поскольку они продолжают производить глюкозу. Наконец, кортизол действует на поджелудочную железу, снижая уровень инсулина и увеличивая уровень глюкагона. Глюкагон представляет собой пептидный гормон, секретируемый альфа-клетками поджелудочной железы для усиления гликогенолиза в печени, глюконеогенеза в печени, кетогенеза в печени, липолиза, а также для снижения липогенеза. Кортизол усиливает активность глюкагона, адреналина и других катехоламинов.
Кортизол усиливает активность глюкагона, адреналина и других катехоламинов.
Механизм
Высвобождение кортизола находится под контролем оси гипоталамус-гипофиз-надпочечники (ГГН). Кортикотропин-рилизинг-гормон (CRH) высвобождается паравентрикулярным ядром (PVN) гипоталамуса.[2] Затем он действует на переднюю долю гипофиза, высвобождая адренокортикотропный гормон (АКТГ), который впоследствии действует на кору надпочечников. В петле отрицательной обратной связи достаточное количество кортизола ингибирует высвобождение как АКТГ, так и КРГ. Ось HPA следует циркадному ритму. Таким образом, уровень кортизола будет высоким утром и низким ночью [2].
Стероидные гормоны, такие как кортизол, являются первичными мессенджерами. Они могут проникать через цитоплазматическую мембрану благодаря своим жирорастворимым свойствам. Клеточные мембраны состоят из двойных слоев фосфолипидов; они предотвращают прохождение жиронерастворимых молекул. Как только кортизол проходит через клеточную мембрану и проникает в клетку, он связывается со специфическими рецепторами в цитоплазме. В отсутствие кортизола глюкокортикоидный рецептор связывается с белком-шапероном Hsp90 в цитозоле. Связывание кортизола с глюкокортикоидным рецептором диссоциирует Hsp9.0. Затем комплекс кортизол-рецептор проникает в ядро клетки и влияет на транскрипцию генов.
В отсутствие кортизола глюкокортикоидный рецептор связывается с белком-шапероном Hsp90 в цитозоле. Связывание кортизола с глюкокортикоидным рецептором диссоциирует Hsp9.0. Затем комплекс кортизол-рецептор проникает в ядро клетки и влияет на транскрипцию генов.
Связанные тесты
Считается, что уровни кортизола в слюне коррелируют с уровнями свободного кортизола в плазме и сыворотке.[6] Ночное измерение кортизола в слюне используется в качестве начального диагностического теста на синдром Кушинга, синдром избытка глюкокортикоидов.[6] Поскольку уровни кортизола должны быть высокими по утрам, одним из первоначальных диагностических тестов на болезнь Аддисона является проверка уровня кортизола в сыворотке рано утром.[9]]
Клиническое значение
Уровень кортизола в организме постоянно контролируется для поддержания гомеостаза. Нерегулируемые уровни могут быть вредными.
Гиперкортицизм
Синдром Кушинга возникает, когда организм человека подвергается воздействию высоких уровней кортизола в течение длительного периода времени. Различные этиологии синдрома Кушинга можно разделить на АКТГ-зависимые и АКТГ-независимые. При АКТГ-зависимых подтипах наблюдается избыток АКТГ либо из-за опухоли гипофиза, либо из-за эктопического источника, такого как нейроэндокринная опухоль.[10] В обоих случаях перепроизводство АКТГ стимулирует надпочечники к выработке избыточного кортизола. В АКТГ-независимых подтипах есть эндогенная этиология и экзогенная этиология. Эндогенная причина обычно связана с опухолью надпочечников, что приводит к избыточной выработке кортизола. Экзогенная причина связана с чрезмерным использованием пероральных или инъекционных кортикостероидов. Пероральные кортикостероиды, такие как преднизолон, увеличивают количество кортизола в организме. Их назначают для облегчения симптомов, связанных с хроническими воспалительными заболеваниями, такими как системная эритематозная волчанка (СКВ) и ревматоидный артрит. Симптомы синдрома Кушинга зависят от того, насколько повышен уровень кортизола. Общие признаки и симптомы избытка кортизола включают увеличение веса (особенно на лице и животе), жировые отложения между лопатками, диабет, гипертонию, гирсутизм у женщин, слабость проксимальных мышц и остеопороз.
Различные этиологии синдрома Кушинга можно разделить на АКТГ-зависимые и АКТГ-независимые. При АКТГ-зависимых подтипах наблюдается избыток АКТГ либо из-за опухоли гипофиза, либо из-за эктопического источника, такого как нейроэндокринная опухоль.[10] В обоих случаях перепроизводство АКТГ стимулирует надпочечники к выработке избыточного кортизола. В АКТГ-независимых подтипах есть эндогенная этиология и экзогенная этиология. Эндогенная причина обычно связана с опухолью надпочечников, что приводит к избыточной выработке кортизола. Экзогенная причина связана с чрезмерным использованием пероральных или инъекционных кортикостероидов. Пероральные кортикостероиды, такие как преднизолон, увеличивают количество кортизола в организме. Их назначают для облегчения симптомов, связанных с хроническими воспалительными заболеваниями, такими как системная эритематозная волчанка (СКВ) и ревматоидный артрит. Симптомы синдрома Кушинга зависят от того, насколько повышен уровень кортизола. Общие признаки и симптомы избытка кортизола включают увеличение веса (особенно на лице и животе), жировые отложения между лопатками, диабет, гипертонию, гирсутизм у женщин, слабость проксимальных мышц и остеопороз. [11] Лечение синдрома Кушинга зависит от причины. Чаще всего лечение проводится с помощью хирургического вмешательства. Однако антагонисты глюкокортикоидных рецепторов также могут применяться при наличии противопоказаний к хирургическому вмешательству.
[11] Лечение синдрома Кушинга зависит от причины. Чаще всего лечение проводится с помощью хирургического вмешательства. Однако антагонисты глюкокортикоидных рецепторов также могут применяться при наличии противопоказаний к хирургическому вмешательству.
Гипокортицизм
Первичная надпочечниковая недостаточность, также известная как болезнь Аддисона, чаще всего вызывается аутоиммунным адреналитом.[9] Другие причины включают злокачественное новообразование, инфекцию или кровоизлияние в надпочечники. Аутоиммунный адреналит возникает в результате того, что организм атакует кору надпочечников.[12] Вторичная недостаточность надпочечников связана с недостаточной продукцией АКТГ передней долей гипофиза. Это может быть вызвано заболеванием гипофиза, но наиболее частая причина связана с подавлением оси HPA из-за хронического приема экзогенных глюкокортикоидов. Третичная надпочечниковая недостаточность возникает из-за отсутствия высвобождения КРГ из гипоталамуса. Симптомы надпочечниковой недостаточности включают утомляемость, потерю веса, гипотонию и гиперпигментацию кожи. [14] Поскольку альдостерона также будет недостаточно, лабораторные результаты покажут гиперкалиемию. Заместительная терапия глюкокортикоидами, например гидрокортизоном, необходима для лечения симптомов гипокортицизма. Важно помнить об увеличении дозировки при острых стрессовых факторах, таких как болезнь или хирургическое вмешательство, чтобы избежать надпочечникового кризиса.[14]
[14] Поскольку альдостерона также будет недостаточно, лабораторные результаты покажут гиперкалиемию. Заместительная терапия глюкокортикоидами, например гидрокортизоном, необходима для лечения симптомов гипокортицизма. Важно помнить об увеличении дозировки при острых стрессовых факторах, таких как болезнь или хирургическое вмешательство, чтобы избежать надпочечникового кризиса.[14]
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Ссылки
- 1.
Ангелуси А., Маргиорис А.Н., Цацанис С. Действие АКТГ на надпочечники. Пришли: Фейнгольд К.Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж., Калра С., Калтсас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы.
 Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342]
Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342]- 2.
Рамамурти С., Сидловски Дж.А. Кортикостероиды: механизмы действия в норме и при заболевании. Реум Дис Клин Норт Ам. 2016 Feb;42(1):15-31, vii. [Бесплатная статья PMC: PMC4662771] [PubMed: 26611548]
- 3.
Kadmiel M, Cidlowski JA. Сигнализация глюкокортикоидных рецепторов в норме и при патологии. Trends Pharmacol Sci. 2013 сен; 34 (9): 518-30. [Бесплатная статья PMC: PMC3951203] [PubMed: 23953592]
- 4.
Oakley RH, Cidlowski JA. Биология глюкокортикоидного рецептора: новые сигнальные механизмы в норме и при патологии. J Аллергия Клин Иммунол. 2013 ноябрь; 132(5):1033-44. [Бесплатная статья PMC: PMC4084612] [PubMed: 24084075]
- 5.
Хакамата Ю., Коми С., Моригути Ю., Изава С., Мотомура Ю., Сато Э., Мизуками С., Ким Ю., Ханакава Т., Иноуэ Ю., Тагая Х. Функциональная связность миндалевидного тела влияет на суточную концентрацию кортизола : предполагаемая связь с тревогой.
 Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810]
Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810]- 6.
Lee DY, Kim E, Choi MH. Технические и клинические аспекты кортизола как биохимического маркера хронического стресса. Отчет BMB, апрель 2015 г.; 48 (4): 209-16. [Бесплатная статья PMC: PMC4436856] [PubMed: 25560699]
- 7.
Kuo T, McQueen A, Chen TC, Wang JC. Регуляция гомеостаза глюкозы глюкокортикоидами. Adv Exp Med Biol. 2015;872:99-126. [Бесплатная статья PMC: PMC6185996] [PubMed: 26215992]
- 8.
Exton JH. Регуляция глюконеогенеза глюкокортикоидами. Моногр Эндокринол. 1979; 12:535-46. [PubMed: 386091]
- 9.
Michels A, Michels N. Болезнь Аддисона: раннее выявление и принципы лечения. Ам семейный врач. 2014 01 апреля; 89(7): 563-8. [PubMed: 24695602]
- 10.
Рафф Х., Кэрролл Т. Синдром Кушинга: от физиологических принципов к диагностике и клиническому лечению.
 Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800]
Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800]- 11.
Лила А.Р., Саратхи В., Джагтап В.С., Бандгар Т., Менон П., Шах Н.С. Синдром Кушинга: поэтапный подход к диагностике. Индийский J Endocrinol Metab. 2011 Октябрь; 15 Дополнение 4 (Приложение 4): S317-21. [Бесплатная статья PMC: PMC3230095] [PubMed: 22145134]
- 12.
Ниари Н., Ниман Л. Надпочечниковая недостаточность: этиология, диагностика и лечение. Curr Opin Endocrinol Diabetes Obes. 2010 июнь;17(3):217-23. [Бесплатная статья PMC: PMC2928659] [PubMed: 20375886]
- 13.
Войцик М., Русала А., Янус Д., Старжик Дж. Б. Вторичная надпочечниковая недостаточность вследствие внутрисуставных инъекций глюкокортикоидов. Индийский педиатр. 2019 15 марта; 56 (3): 242-243. [PubMed: 30954999]
- 14.
Александраки К.И., Санпавитаякул К., Гроссман А. Надпочечниковая недостаточность. Пришли: Фейнгольд К.


 Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342]
Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342] Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810]
Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810] Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800]
Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800] Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж., Калра С., Калтсас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы. Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 7 ноября 2022 г. [PubMed: 25905309]
Р., Анавальт Б., Блэкман М.Р., Бойс А., Хрусос Г., Корпас Э., де Гердер В.В., Дхатария К., Дунган К., Хофланд Дж., Калра С., Калтсас Г., Капур Н., Кох К., Копп П., Корбонитс М. , Kovacs CS, Kuohung W, Laferrere B, Levy M, McGee EA, McLachlan R, New M, Purnell J, Sahay R, Shah AS, Singer F, Sperling MA, Stratakis CA, Trance DL, Wilson DP, редакторы. Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 7 ноября 2022 г. [PubMed: 25905309] Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342]
Эндотекст [Интернет]. MDText.com, Inc.; Южный Дартмут (Массачусетс): 13 июня 2020 г. [PubMed: 25905342] Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810]
Научный представитель 2017 г. 16 августа; 7 (1): 8313. [Бесплатная статья PMC: PMC5559590] [PubMed: 28814810] Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800]
Дж. Физиол. 2015 01 февраля; 593 (3): 493-506. [Бесплатная статья PMC: PMC4324701] [PubMed: 25480800]